Cho Zn, Al tác dụng với HCL, hỏi chất nào giải phóng khí H2 ra nhiều hơn?
(mình đang cần gấp, mấy bạn giải nhanh giúp mình với:<)
có ai biết giải bài giải bài này ko giúp mình với mình đang cần rất rất gấp mong các bạn giúp cho
Bài 1: cho các chất sau: CuO, Na2SO3, Al, Fe2O3,NO, Fe(OH)3 . Hãy chon 1 trong các chất đã cho tác dụng với axit sunfuric loãng sinh ra:
a, khí nặng hơn không khí và gây nên hiện tượng mưa axit
b, dd có màu xanh lam
c, dd có màu vàng nâu
d, dd ko có màu
viết PTHH xảy ra
Bài 2: cho các axit sau: FeO, SO2, CO, MgO, CO2.
a, oxit nào tác dụng được với dd axit clohidric
b, oxit nào t/d đc với dd kali hiđrôxit
c, oxit nào t/d vs nước
Viết PTHH
Bài 3: cho V lit khí sunfuro (ĐKTC) t/d vừa đủ với 200ml Ca(OH)2 nồng độ 0,5M tạo muối trung hòa.
a, Viết PTHH
b, Tính giá trị của V
c, tính khối lượng muối tạo thành.
Bài 1 :
a) Khí đó là $SO_2$
$Na_2SO_3 + H_2SO_4 \to Na_2SO_4 + SO_2 + H_2O$
b) Dung dịch đó là $CuSO_4$
$CuO + H_2SO_4 \to CuSO_4 + H_2O$
c) Dung dịch đó là $Fe_2(SO_4)_3$
$Fe_2O_3 + 3H_2SO_4 \to Fe_2(SO_4)_3 + 3H_2O$
$2Fe(OH)_3 + 3H_2SO_4 \to Fe_2(SO_4)_3 + 6H_2O$
d) Dung dịch đó là : $Al_2(SO_4)_3$
$2Al + 3H_2SO_4 \to Al_2(SO_4)_3 + 3H_2$
Bài 2 :
a)
$FeO + 2HCl \to FeCl_2 + H_2O$
$MgO + 2HCl \to MgCl_2 + H_2O$
b)
$SO_2 + KOH \to KHSO_3$
$CO_2 + KOH \to KHCO_3$
c)
$SO_2 + H_2O \rightleftharpoons H_2SO_3$
$CO_2 + H_2O \rightleftharpoons H_2CO_3$
Bài 3 :
a) $Ca(OH)_2 + SO_2 \to CaSO_3 + H_2O$
b) $n_{SO_2} = n_{Ca(OH)_2} = 0,2.0,5 = 0,1(mol)$
$V = 0,1.22,4 = 2,24(lít)$
c) $n_{CaSO_3} = n_{Ca(OH)_2} = 0,1(mol)$
$m_{CaSO_3} = 0,1.120 = 12(gam)$
có ai bt giải bai này k mình đang cần rất rất gấp mong các bạn giúp cho
Bài 2: cho các chất sau : Cu(OH)2 , ZN, Al2O3, Fe2O3, Fe(OH)3 . hãy chọn một trong các chất đã cho tác dụng với axit clohidric (HCL) sinh ra
a, khí nhẹ hơn kk và cháy đc trong kk
b, dd có màu xanh lam
c, dd có màu vàng nâu
d, dd không có màu
viết PTHH xảy ra
Bài 2 :
a) Khí nhẹ hơn không khí và cháy được trong không khí :
Pt : Zn + 2HCl → ZnCl2 + H2
b) Dung dịch có màu xanh lam :
Pt : Cu(OH)2 + 2HCl → CuCl2 + 2H2O
c) Dung dịch có màu vàng nâu :
Pt : Fe(OH)3 + 3HCl → 2FeCl3 +3H2O
d) Dung dịch không màu :
Pt : Al2O3 + 6HCl → 2AlCl3 + 3H2O
Chúc bạn học tốt
a) Sơ đồ phản ứng : \(HCl+Zn-->ZnCl_2+H_2\)
Phương trình hóa học : \(2HCl+Zn\rightarrow ZnCl_2+H_2\uparrow\)
b) Số mol HCl tham gia phản ứng :
\(n_{HCl}=\frac{m_{HCl}}{M_{HCl}}=\frac{14,6}{36,5}=0,4\left(mol\right)\)
Theo PTHH :
2 mol HCl tham gia phản ứng tạo thành 1 mol H2
=> 0, 4 mol HCl tham gia phản ứng tạo thành 0, 2 mol H2
Thể tích khí H2 thu được ở đktc là :
\(V_{H_2}=n_{H_2}\cdot22,4=0,2\cdot22,4=4,48\left(l\right)\)
cho 31,4 g hỗn hợp G gồm Al và Zn tác dụng vừa đủ với dung dịch HCl 2M thu được 15,68 (l) H2 (đktc).
a.tính % khối lượng từng chất trong G.
b.tính thể tích HCl đã dùng.
giải rõ ràng ra dùm mình cần gấp tối nay lúc 1030 giúp dùm mình cần rất gấp
a) Ta có: \(n_{H_2}=\dfrac{15,68}{22,4}=0,7\left(mol\right)\)
Gọi a và b lần lượt là số mol của Al và Zn
Bảo toàn mol e: \(3a+2b=1,4\)
Mà \(27a+65b=31,4\)
\(\Rightarrow\left\{{}\begin{matrix}a=0,2\\b=0,4\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}\%m_{Al}=\dfrac{0,2\cdot27}{31,4}\cdot100\%\approx17,2\%\\\%m_{Zn}=82,8\%\end{matrix}\right.\)
b) Bảo toàn nguyên tố: \(n_{HCl}=2n_{H_2}=1,4mol\)
\(\Rightarrow V_{HCl}=\dfrac{1,4}{2}=0,7\left(l\right)=700\left(ml\right)\)
Đặt :
nAl = a mol
nZn = b mol
mB = 27a + 65b = 31.4 (g) (1)
2Al + 6HCl => 2AlCl3 + 3H2
a___________________1.5a
Zn + 2HCl => ZnCl2 + H2
b__________________b
nH2 = 1.5a + b = 15.68/22.4 = 0.7 (mol) (2)
(1) , (2) :
a = 0.2
b = 0.4
%Al = 5.4/31.4 * 100% = 17.19%
%Zn = 100 - 17.19 = 82.81%
nHCl = 2nH2 = 0.7*2 = 1.4 (mol)
Vdd HCl = 1.4 / 2 = 0.7 (l)
Chia 39,9 gam hỗn hợp X ở dạng bột gồm Na, Al, Fe thành ba phần bằng nhau:
- Phần 1: cho tác dụng với nước dư, giải phóng ra 4,48 lít khí H2.
- Phần 2: Cho tác dụng với dung dịch NaOH dư, giải phóng ra 7,84 lít khí H2.
- Phần 3: Cho vào dung dịch HCl dư, thấy giải phóng ra V lít khí H2 (các khí đo ở đktc). Giá trị của V là?
A. 7,84
B. 13,44
C. 10,08.
D. 12,32.
Chia 39,9 gam hỗn hợp X ở dạng bột gồm Na, Al, Fe thành ba phần bằng nhau :
- Phần 1: cho tác dụng với nước dư, giải phóng ra 4,48 lít khí H2.
- Phần 2: Cho tác dụng với dung dịch NaOH dư, giải phóng ra 7,84 lít khí H2.
- Phần 3: Cho vào dung dịch HCl dư, thấy giải phóng ra V lít khí H2 (các khí đo ở đktc). Giá trị của V là ?
A. 7,84.
B. 13,44.
C. 10,08.
D. 12,32.
Đáp án C
Đặt nAl = x; nNa = y ; nFe = z (mol)
P2 tác dụng với NaOH dư cho nhiều khí hơn P1
=>P1 Al chưa tan hết.
Ta có: mhh = 27x + 23y + 56z = 39,9
n khí P1 = y 2 + 3 y 2 = 0 , 2
n khí P2 = y 2 + 3 x 2 = 0 , 35
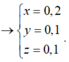
Vậy nếu t/d với dung dịch HCl thì ånkhí =
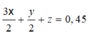
V = 0,45.22,4 = 10,08 lít
Chia 39,9 gam hỗn hợp X ở dạng bột gồm Na, Al, Fe thành ba phần bằng nhau :
- Phần 1: cho tác dụng với nước dư, giải phóng ra 4,48 lít khí H2.
- Phần 2: Cho tác dụng với dung dịch NaOH dư, giải phóng ra 7,84 lít khí H2.
- Phần 3: Cho vào dung dịch HCl dư, thấy giải phóng ra V lít khí H2 (các khí đo ở đktc). Giá trị của V là ?
A. 7,84
B. 13,44
C. 10,08
D. 12,32
Chia 39,9 gam hỗn hợp X ở dạng bột gồm Na, Al, Fe thành ba phần bằng nhau :
- Phần 1: cho tác dụng với nước dư, giải phóng ra 4,48 lít khí H2.
- Phần 2: Cho tác dụng với dung dịch NaOH dư, giải phóng ra 7,84 lít khí H2.
- Phần 3: Cho vào dung dịch HCl dư, thấy giải phóng ra V lít khí H2 (các khí đo ở đktc). Giá trị của V là ?
A. 7,84
B. 13,44
C. 10,08
D. 12,32
Chia 39,9 gam hỗn hợp X ở dạng bột gồm Na, Al, Fe thành ba phần bằng nhau :
- Phần 1: cho tác dụng với nước dư, giải phóng ra 4,48 lít khí H2.
- Phần 2: Cho tác dụng với dung dịch NaOH dư, giải phóng ra 7,84 lít khí H2.
- Phần 3: Cho vào dung dịch HCl dư, thấy giải phóng ra V lít khí H2 (các khí đo ở đktc). Giá trị của V là ?
A. 7,84.
B. 13,44.
C. 10,08.
D. 12,32.
Đáp án C
Đặt nAl = x; nNa = y ; nFe = z (mol)
P2 tác dụng với NaOH dư cho nhiều khí hơn P1
=>P1 Al chưa tan hết.
Ta có: mhh = 27x + 23y + 56z = 39,9
n khí P1 = y 2 + 3 y 2 = 0,2
n khí P2 = y 2 + 3 x 2 = 0,35
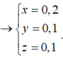
Vậy nếu t/d với dung dịch HCl thì ånkhí = 3 x 2 + y 2 + z = 0 , 45 mol
V = 0,45.22,4 = 10,08 lít